
News
Zusammen ist besser als allein: Wie ein altbekannter Wirkstoff zum Gamechanger werden kann
13.04.2022 / Zur Behandlung von COVID-19 stehen immer mehr Medikamente zur Verfügung. Berliner Forschende von Charité, FU und MDC haben die Wirkmechanismen von antiviralen und anti-entzündlichen Substanzen untersucht. Im Journal „Molecular Therapy“ beschreiben sie, dass eine Kombination aus beiden am besten funktioniert.
Noch immer führen Infektionen mit SARS-CoV-2 auch zu Aufnahmen in ein Krankenhaus. Derzeit werden laut Robert-Koch-Institut innerhalb einer Woche pro 100.000 Einwohner*innen etwa sechs bis sieben Menschen mit COVID-19 eingewiesen. Bei der stationären Behandlung von COVID-19-Patient*innen gibt es mittlerweile eine Reihe von Medikamenten, die den Krankheitsverlauf abmildern oder bei Schwerkranken das Risiko eines tödlichen Verlaufs verringern. Einige bekämpfen das Virus, andere die Entzündung, die es hervorruft.
Besonders werden monoklonale Antikörper und das stark entzündungshemmende Medikament Dexamethason eingesetzt. Antikörper fangen das Virus ab, heften sich an die Oberfläche des Spikeproteins und verhindern so, dass es in die menschlichen Zellen eintritt. Diese Therapie wird bis zum siebten Tag nach Beginn der Symptome angewandt. Sauerstoffpflichtige COVID-19-Patient*innen im Krankenaus erhalten in der Regel Dexamethason. Das Glukokortikoid hat sich seit etwa 60 Jahren bei einigen, auf einer übermäßigen Aktivierung des Immunsystems beruhenden Entzündungen bewährt. Auch bei COVID-19 dämpft es die Entzündungsreaktion des Körpers zuverlässig. Allerdings geht der Wirkstoff mit verschiedenen Nebenwirkungen einher, so kann er beispielsweise Pilzinfektionen nach sich ziehen. Deshalb sollte das Mittel nur sehr gezielt eingesetzt werden.
Schwerer Verlauf beim Zwerghamster
Wissenschaftler*innen der Charité, des Berliner Instituts für Medizinische Systembiologie (BIMSB) am Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft (MDC) und der FU Berlin haben die Wirkmechanismen beider Therapien untersucht. „Dabei haben wir Hinweise dafür gefunden, dass eine Kombination aus Antikörper- und Dexamethason-Therapie besser wirkt als die einzelnen Therapien für sich genommen“, sagt Dr. Emanuel Wyler, Wissenschaftler der Arbeitsgruppe RNA Biologie und Posttranscriptionale Regulation unter Leitung von Prof. Dr. Markus Landthaler am BIMSB, und Erstautor der Studie. Da nicht alle Lungenareale anhand von Proben von Patient*innen untersucht werden können, suchten die Forschungsteams im vergangenen Jahr zunächst nach einem geeigneten Modell. Co-Letztautor Dr. Jakob Trimpert, Tiermediziner und Arbeitsgruppenleiter am Institut für Virologie der Freien Universität Berlin, entwickelte in diesem Zuge COVID-19-Hamstermodelle. Die Tiere sind derzeit der wichtigste nicht transgene Modellorganismus für COVID-19, da sie sich mit denselben Virusvarianten wie Menschen infizieren und ähnliche Krankheitssymptome entwickeln. Die Erkrankung läuft bei den einzelnen Arten unterschiedlich ab: Goldhamster erkranken nur moderat, während Roborovski-Zwerghamster einen schweren Verlauf zeigen, der dem von COVID-19-Patient*innen auf Intensivstationen ähnelt.
Zusammenspiel der Signalwege
„In der aktuellen Studie haben wir die Auswirkungen von separaten und kombinierten antiviralen und entzündungshemmenden Behandlungen für COVID-19, also mit monoklonalen Antikörpern, Dexamethason oder einer Kombination aus beiden Therapien, in den vorhandenen Modellen geprüft“, erklärt Dr. Trimpert. Um das Ausmaß der Schädigung des Lungengewebes zu analysieren, untersuchten die Veterinärpathologen der FU Berlin infiziertes Lungengewebe unter dem Mikroskop. Außerdem bestimmte das Team um Dr. Trimpert zu verschiedenen Zeitpunkten der Behandlung die Menge an infektiösen Viren und Virus-RNA. So konnten die Wissenschaftler*innen überprüfen, ob und wie sich die Virenaktivität im Lauf der Therapie veränderte. „Mithilfe von detaillierten Analysen verschiedener Parameter einer COVID-19-Erkrankung, die so nur im Tiermodell möglich sind, ist es uns gelungen, nicht nur die Grundlagen der Wirkungsweise von zwei besonders wichtigen COVID-19-Medikamenten besser zu verstehen, wir fanden auch deutliche Hinweise auf mögliche Vorteile einer Kombinationstherapie aus monoklonalen Antikörpern und Dexamethason“, sagt Dr. Trimpert.
Den Einfluss der Medikamente auf das komplexe Zusammenspiel der Signalwege innerhalb der Gewebezellen und auf die Anzahl der Immunzellen haben Einzelzellanalysen gezeigt. Dabei lassen die Forschenden die einzelnen Zellen einer Probe über einen Chip laufen. Dort werden sie zusammen mit einem Barcode in kleine wässrige Tröpfchen verpackt. Auf diese Weise kann die RNA – der Teil des Erbgutes, den die Zelle gerade abgelesen hatte – sequenziert und später der Zelle wieder zugeordnet werden. Aus den gewonnenen Daten lässt sich mit hoher Präzision auf die Funktion der Zelle schließen. „So konnten wir beobachten, dass die Antikörper die Virusmenge effizient reduzieren konnten“, erläutert Dr. Wyler. „Im Modell half das jedoch nicht viel.“ Denn nicht die Viren schädigen das Lungengewebe, sondern die starke Entzündungsreaktion, die sie auslösen. Die Immunzellen, die die Eindringlinge bekämpfen, schütten Botenstoffe aus, um Verstärkung herbeizurufen. Die Massen an Abwehrkämpfern, die herbeiströmen, können die Lunge regelrecht verstopfen. „Verschlossene Blutgefäße und instabile Gefäßwände können dann zu einem akuten Lungenversagen führen“, erklärt der Wissenschaftler.
Bekannter Wirkstoff als Gamechanger?
Für eine Überraschung sorgte das altbekannte Dexamethason. „Der Entzündungshemmer wirkt ganz besonders stark auf eine bestimmte Art von Immunzellen, die Neutrophilen“, sagt Co-Letztautorin Dr. Geraldine Nouailles, wissenschaftliche Arbeitsgruppenleiterin an der Medizinischen Klinik mit Schwerpunkt Infektiologie und Pneumologie der Charité. Die Neutrophilen gehören zu den weißen Blutkörperchen und treten bei Infektionen mit Viren und Bakterien sehr schnell auf den Plan. „Das Kortison-Präparat unterdrückt das Immunsystem und hindert die Neutrophilen daran, Botenstoffe zu produzieren, die andere Immunzellen anlocken“, führt Dr. Nouailles aus. „So verhindert das Medikament sehr effektiv eine Eskalation der Immunabwehr.“
Die besten Behandlungsergebnisse erreichten die Forschenden, als sie die anti-virale mit der anti-entzündlichen Therapie kombinierten. „Eine solche Kombinationstherapie sehen die medizinischen Leitlinien bislang nicht vor“, betont Dr. Nouailles. „Hinzu kommt, dass eine Antikörpertherapie bislang nur bis zum maximal siebten Tag nach Symptombeginn bei Hochrisikopatient*innen verabreicht werden darf. Dexamethason wird in der Praxis erst verabreicht, wenn die Patient*innen sauerstoffpflichtig werden, also ihre Erkrankung bereits weit fortgeschritten ist. In der Kombination hingegen eröffnen sich ganz neue Zeitfenster der Behandlung.“ Ein Ansatz, der nun in klinischen Studien überprüft werden muss, bevor er für die Behandlung von Patient*innen infrage kommt.
Weitere Informationen
Arbeitsgruppe von Prof. Markus Landthaler
Medizinische Klinik mit Schwerpunkt Infektiologie und Pneumologie
Fachbereich Veterinärmedizin der FU Berlin
Pressemitteilung zu vorangegangener Publikation 08/2021 in Nature Communications
Über die Studie
Gefördert wurden die Arbeiten unter anderem durch die Deutsche Forschungsgemeinschaft (DFG) im Sonderforschungsbereich SFB-TR84, das Bundesministerium für Bildung und Forschung (BMBF) mit den Projekten CAPSyS-COVID sowie PROVID und das Berlin Institute of Health (BIH) in der Charité mit CM-COVID. Ebenfalls ermöglicht hat die Studie das BMBF-geförderte Nationale Forschungsnetzwerk der Universitätsmedizin zu Covid-19 (NUM), im Teilvorhaben Organostrat.
Literatur
Emanuel Wyler et al (2022): „Key benefits of dexamethasone and antibody treatment in COVID-19 hamster models revealed by single cell transcriptomics “, in: Molecular Therapy, DOI: https://doi.org/10.1016/j.ymthe.2022.03.014
Max-Delbrück-Centrum für Molekulare Medizin (MDC)
Das Max-Delbrück-Centrum für Molekulare Medizin in der Helmholtz-Gemeinschaft gehört zu den international führenden biomedizinischen Forschungszentren. Nobelpreisträger Max Delbrück, geboren in Berlin, war ein Begründer der Molekularbiologie. An den MDC-Standorten in Berlin-Buch und Mitte analysieren Forscher*innen aus rund 60 Ländern das System Mensch – die Grundlagen des Lebens von seinen kleinsten Bausteinen bis zu organübergreifenden Mechanismen. Wenn man versteht, was das dynamische Gleichgewicht in der Zelle, einem Organ oder im ganzen Körper steuert oder stört, kann man Krankheiten vorbeugen, sie früh diagnostizieren und mit passgenauen Therapien stoppen. Die Erkenntnisse der Grundlagenforschung sollen rasch Patient*innen zugutekommen. Das MDC fördert daher Ausgründungen und kooperiert in Netzwerken. Besonders eng sind die Partnerschaften mit der Charité – Universitätsmedizin Berlin im gemeinsamen Experimental and Clinical Research Center (ECRC) und dem Berlin Institute of Health (BIH) in der Charité sowie dem Deutschen Zentrum für Herz-Kreislauf-Forschung (DZHK). Am MDC arbeiten 1600 Menschen. Finanziert wird das 1992 gegründete MDC zu 90 Prozent vom Bund und zu 10 Prozent vom Land Berlin.
Über die Charité – Universitätsmedizin Berlin
Die Charité – Universitätsmedizin Berlin ist mit rund 100 Kliniken und Instituten an vier Campi sowie 3.001 Betten eine der größten Universitätskliniken Europas. Forschung, Lehre und Krankenversorgung sind hier eng miteinander vernetzt. Mit Charité-weit durchschnittlich 16.391 und konzernweit rund 19.400 Beschäftigten aus über 100 Nationen gehört die Berliner Universitätsmedizin zu den größten Arbeitgeberinnen der Hauptstadt. Dabei waren 4.707 der Beschäftigten im Pflegebereich und 4.693 im wissenschaftlichen und ärztlichen Bereich tätig. An der Charité wurden im vergangenen Jahr 132.383 voll- und teilstationäre Fälle sowie 655.138 ambulante Fälle behandelt. Im Jahr 2020 hat die Charité Gesamteinnahmen von rund 2,2 Milliarden Euro, inklusive Drittmitteleinnahmen und Investitionszuschüssen, erzielt. Mit den 196 Millionen Euro eingeworbenen Drittmitteln erreichte die Charité einen erneuten Rekord. An der medizinischen Fakultät, die zu den größten in Deutschland gehört, werden mehr als 8.600 Studierende in Humanmedizin, Zahnmedizin sowie Gesundheitswissenschaften ausgebildet. Darüber hinaus gibt es 577 Ausbildungsplätze in 10 Gesundheitsberufen. Die Berliner Universitätsmedizin setzt Akzente in den Forschungsschwerpunkten: Infektion, Inflammation und Immunität einschließlich Forschung zu COVID-19, Kardiovaskuläre Forschung und Metabolismus, Neurowissenschaften, Onkologie, Regenerative Therapien sowie Seltene Erkrankungen und Genetik. Wissenschaftlerinnen und Wissenschaftler der Charité arbeiten unter anderem in 29 DFG-Sonderforschungsbereichen, darunter sechs mit Sprecherfunktion, in drei Exzellenzclustern, davon eines mit Sprecherschaft, 8 Emmy-Noether-Nachwuchsgruppen, 16 Grants des European Research Councils und 9 europäischen Verbundprojekten mit Charité-Koordination.
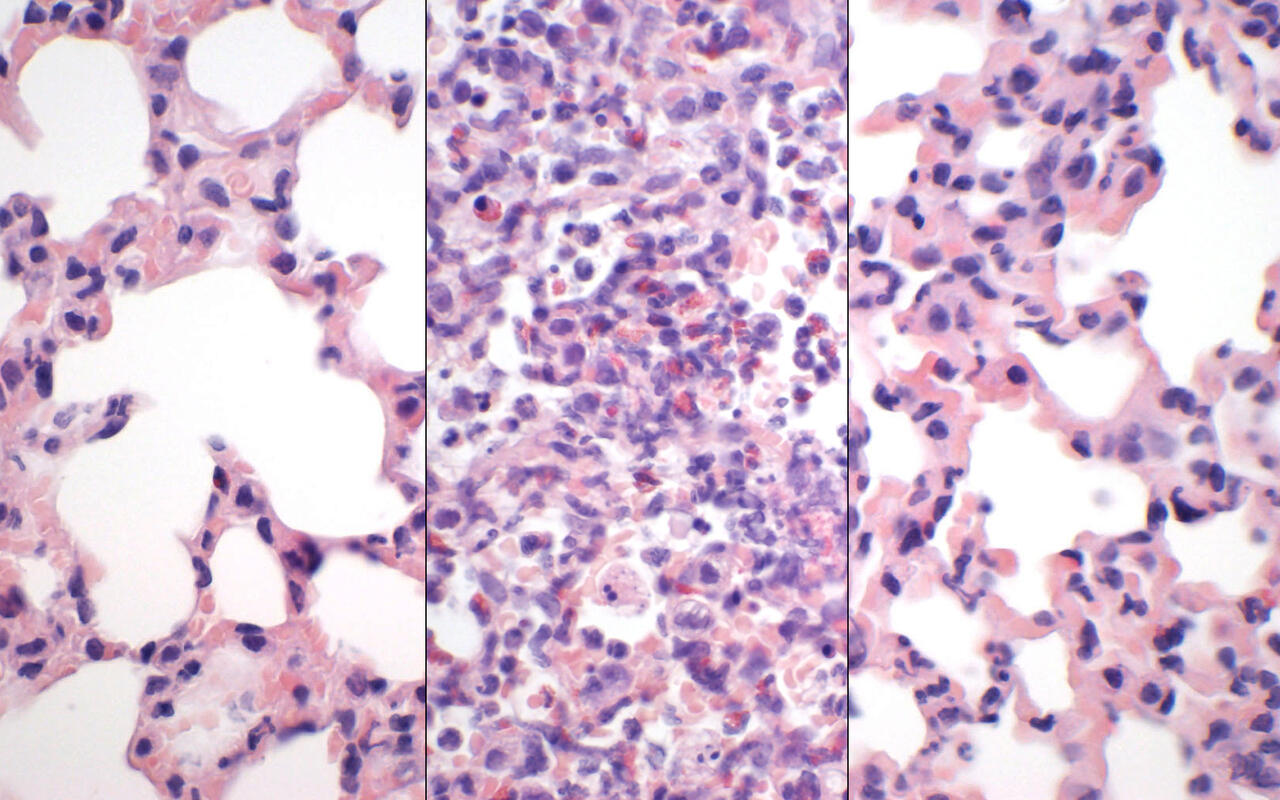
Foto: In jeweils 600-facher Vergrößerung: gesundes Lungengewebe mit offenen Lungenbläschen (links), schwere SARS-CoV-2-Infektion mit zerstörtem Gewebe und Immunzellen (mitte), deutlich weniger Zerstörung und verbesserter Gasaustausch nach Kombinationsbehandlung (rechts).© Judith Bushe/ Anne Voß, FU Berlin
Quelle: Pressemitteilung MDCZusammen ist besser als allein: Wie ein altbekannter Wirkstoff zum Gamechanger werden kann